Contenu:
◉ Introduction
Plasmodium est un parasite hématozoaire, ce qui signifie qu'il infecte les globules rouges du sang. Il est responsable du paludisme (malaria), l'une des infections parasitaires les plus répandues dans le monde.
Le parasite est transmis à l'homme par la piqûre d'un moustique du genre Anopheles, qui est principalement présent dans les régions chaudes.
Il existe plus de 100 espèces de Plasmodium, mais seulement 6 sont pathogènes pour l'homme : Plasmodium falciparum, Plasmodium vivax, Plasmodium malariae, Plasmodium ovale, Plasmodium knowlesi et P. cynomolgi.
Les symptômes du paludisme varient considérablement. Typiquement, ils suivent un cycle caractéristique comprenant des frissons, suivis de fièvre, puis de sueurs. Ce cycle de symptômes se répète généralement tous les 48 à 72 heures, en fonction de l'espèce de Plasmodium.
L'infection par certaines espèces, notamment Plasmodium falciparum, peut être particulièrement grave et potentiellement mortelle si elle n'est traitée rapidement.
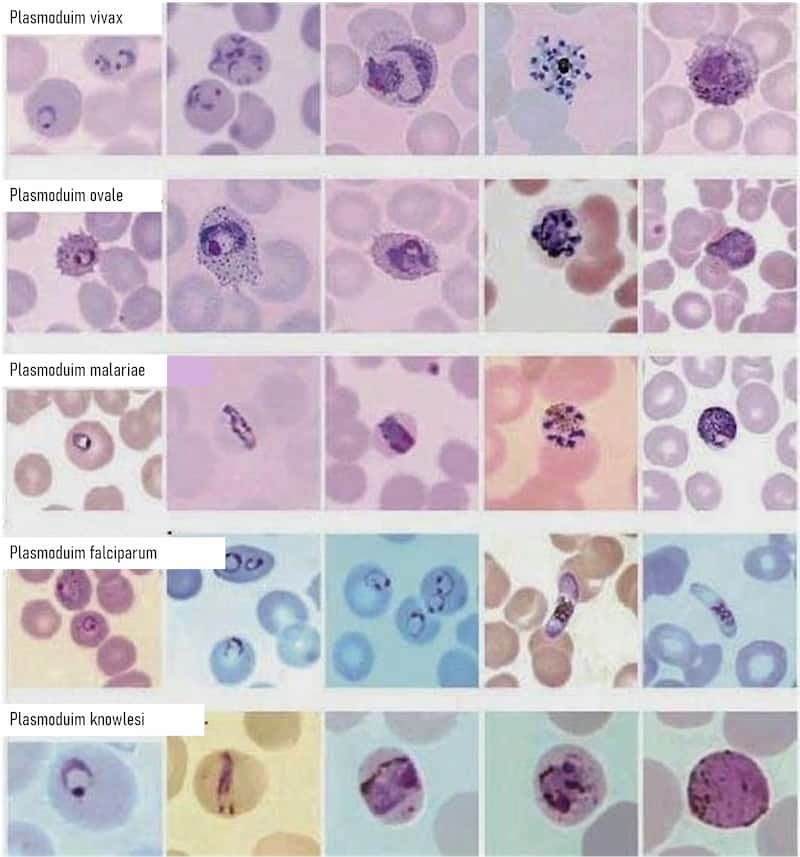
◉ Classification
- Embranchement : Protozoaires (unicellulaires)
- Classe : Sporozoaire.
- Genre : Plasmodium.
- Espèce : 6 espèces pathogènes à l'Homme ;
- P. vivax: la plus fréquente en Algérie, devenue cosmopolite.
- P. malariae : cosmopolite.
- P. ovale: Afrique noire.
- P. falciparum: la plus fréquente (zones tropicales chaudes et humides), la plus redoutable et mortelle.
- P. knowlesi: Asie du sud-est telle que la Malaisie, passée du singe à l'Homme, mortelle.
- P. cynomolgi : Ce parasite semble actuellement géographiquement limité à l'Asie du Sud-Est.
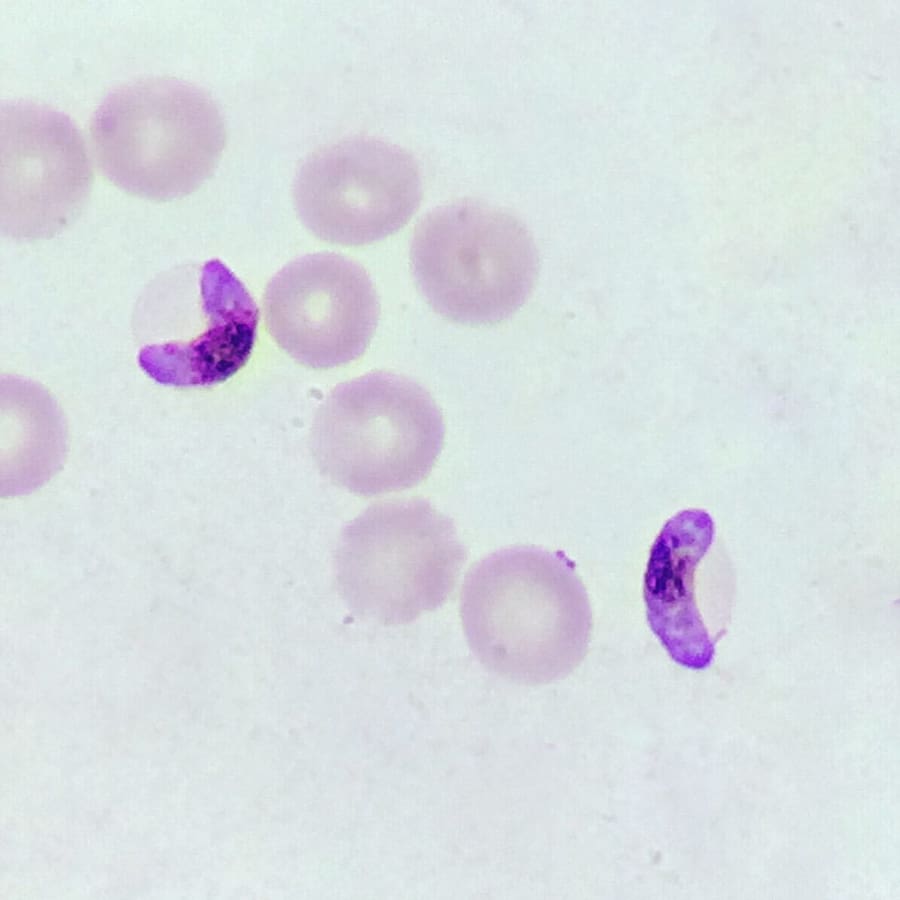
Photo 02: Plasmodium-falciparum
◉ Morphologie
◉ 1. Hypnozoïte
Phase de persistance du parasite au niveau hépatique. Reste en état latent et peut réactiver plus tard pour provoquer des rechutes, principalement dans les infections par Plasmodium vivax et Plasmodium ovale.
◉ 2. Mérozoïte
Forme du parasite qui émerge du foie et entre dans la circulation sanguine. Capable d'infecter les érythrocytes (globules rouges) et de provoquer la phase érythrocytaire du cycle, où il se multiplie.
◉ 3. Trophozoïte
Stade du développement du parasite à l'intérieur des érythrocytes. Se nourrit de l'hémoglobine et évolue en schizonte.
◉ 4. Schizonte
Cellule multinucléée formée à partir du trophozoïte. Une fois mature, le schizonte se rompt et libère 8 à 32 mérozoïtes dans la circulation sanguine, perpétuant ainsi l'infection des globules rouges.
◉ 5. Gamétocytes
Formes sexuelles du parasite présentes dans le sang. Lorsque ingérés par un moustique Anopheles lors d'un repas sanguin, ils se développent en gamètes mâles et femelles dans l'intestin du moustique.
◉ 6. Ookinète
Forme mobile du zygote formé après la fécondation des gamètes dans l'intestin du moustique. Capable de traverser la paroi intestinale du moustique pour former un oocyste.
◉ 7. Oocyste
Forme fixe du parasite qui se développe à l'extérieur de la paroi intestinale du moustique. Une fois mature, il libère de nombreux sporozoïtes dans l'hémolymphe du moustique.
◉ 8. Sporozoïte
Forme infectieuse du parasite pour les mammifères. Migrent vers les glandes salivaires du moustique et sont injectés dans l'hôte humain lors d'une piqûre, initiant ainsi un nouveau cycle d'infection en se dirigeant vers le foie.
◉ Contamination / Transmission
◉ 1. Mode de Contamination
La contamination de l'homme se fait par voie orale, par ingestion de kystes mûrs à 4 noyaux :
- Directement : Par les mains sales.
- Indirectement : En ingérant des aliments (crus, fruits) ou de l'eau souillés par les déjections d'individus infectés.
- Transport passif : Par des mouches qui jouent un rôle phorétique.
◉ 2. Facteurs Favorisants
- Facteurs locaux : Provoquent une irritation mécanique du côlon.
- Alimentation (épices, alcool), purgation.
- Modification de la flore bactérienne intestinale (salmonelles), et des parasites intestinaux (Giardia, helminthes).
- Facteurs généraux : Augmentent la vulnérabilité de l'hôte.
- Stress, refroidissement, surmenage, corticothérapie.
- Facteurs parasitaires : Pathogénicité des souches.
◉ Cycle Évolutif
Le cycle de Plasmodium se déroule successivement chez l'Homme (hôte intermédiaire) et chez le moustique anophèle (hôte définitif). Ces parasites ont deux types de reproduction :
- 1- Reproduction asexuée schizogonique :
- Cycle endo-érythrocytaire : Se déroule dans les hématies (globules rouges) par division binaire ou scissiparité.
- Cycle exo-érythrocytaire : Se déroule dans le foie.
- 2- Reproduction sexuée/sporogonique/gamagonique :
- Se déroule chez le vecteur, l'anophèle femelle.
◉ 1. Phase chez l'Homme (Phase asexuée)
Le cycle asexué chez l'Homme est divisé en deux phases : la phase hépatique (exo-érythrocytaire) et la phase sanguine (érythrocytaire).
Phase exo-érythrocytaire intra-hépatique
- Les sporozoïtes sont injectés dans la peau par l'anophèle femelle lors d'un repas sanguin.
- En moins de 30 minutes, les sporozoïtes atteignent les hépatocytes du foie.
- À l'intérieur des hépatocytes, les sporozoïtes deviennent des cryptozoïtes (ou hypnozoïtes selon les souches).
- Les cryptozoïtes se multiplient et forment des corps bleus (hépatocytes remplis de mérozoïtes).
- Ces corps éclatent, libérant des milliers de mérozoïtes dans le sang.
Phase érythrocytaire
- Les mérozoïtes pénètrent rapidement dans les globules rouges.
- À l'intérieur des globules rouges, les mérozoïtes se transforment en trophozoïtes.
- Les trophozoïtes se multiplient, formant des schizontes, puis des rosaces (globules rouges remplis de mérozoïtes).
- Les globules rouges éclatent, libérant de nouveaux mérozoïtes qui infectent d'autres globules rouges.
- Après plusieurs cycles de schizogonie, certains mérozoïtes se différencient en gamétocytes mâles et femelles.
◉ 2. Phase chez le moustique (Phase sexuée ou sporogonique)
Phase sporogonique
- Lors d'un repas sanguin sur un hôte infecté, le moustique ingère des mérozoïtes, trophozoïtes, schizontes et gamétocytes.
- Dans le tube digestif du moustique, tous les stades sont détruits sauf les gamétocytes.
- Les gamétocytes se transforment en gamètes mâles et femelles, qui fusionnent pour former un ookinète.
- L'ookinète migre et se fixe à la paroi externe de l'estomac du moustique, se transformant en oocyste.
- À l'intérieur de l'oocyste, les cellules se multiplient, produisant des centaines de sporozoïtes.
- Les sporozoïtes migrent vers les glandes salivaires du moustique, prêts à être inoculés dans un nouvel hôte lors d'un prochain repas sanguin.
◉ 2. Cycle Pathogène : Amibiase Maladie
- Transformation : Des changements, comme une modification de la flore intestinale ou une infection, transforment Entamoeba histolytica minuta en Entamoeba histolytica histolytica.
- Invasion : L'amibe pathogène pénètre la muqueuse colique, créant des ulcérations et se multipliant dans la sous-muqueuse, provoquant des abcès.
- Propagation : Les amibes sont généralement rejetées dans l'intestin puis à l'extérieur, mais elles peuvent aussi atteindre le foie via la circulation sanguine, provoquant une amibiase hépatique et parfois infectant les poumons et d'autres organes.
◉ Caractéristiques de la Maladie
◉ Nature systémique
La maladie affecte plusieurs systèmes du corps, pas seulement un organe ou une région spécifique. Cela signifie que les symptômes peuvent varier largement et toucher divers aspects de la santé.
◉ Période d'incubation
Entre 7 et 14 jours après la piqûre d'un moustique infecté, le parasite se multiplie dans le foie avant de passer dans le sang, où il provoque les symptômes.
◉ Déclenchement des symptômes
Les symptômes du paludisme sont dus à la libération de produits, y compris des détritus de cellules sanguines infectées et des substances pyrogènes (qui provoquent de la fièvre), lorsque les parasites éclatent les globules rouges pour continuer leur cycle de vie.
◉ Symptômes caractéristiques
Présentation clinique: La manifestation typique inclut des frissons, suivis de fièvre élevée et de sueurs, et ce cycle dure environ 10 heures.
- Phase de frissons: Le patient ressent un froid intense et des tremblements.
- Phase de fièvre: La température corporelle monte brusquement, souvent accompagnée de maux de tête et de douleurs musculaires.
- Phase de sueurs: La fièvre retombe, causant une transpiration abondante.
◉ Tendance à la chronicité
- Latence et rechutes: Après le traitement initial ou une phase aiguë, la maladie peut entrer en phase de latence où les symptômes disparaissent temporairement.
- Rechutes: Les parasites peuvent rester dormants dans le foie et réactiver plus tard, causant de nouveaux épisodes de symptômes. Cette rechute peut se produire des semaines, des mois, voire des années après l'infection initiale.
◉ Diagnostic
◉ 1. Diagnostic Direct
Recherche directe du parasite dans le sang sur frottis et goutte épaisse:
1. 1 Frottis sanguin
Considéré comme la référence en matière de diagnostic, cette méthode consiste à colorer un frottis sanguin avec du colorant de Giemsa et à l'examiner au microscope. Utilisé pour identifier les hématozoaires et distinguer les différents stades intra-érythrocytaires de Plasmodium, permettant ainsi un diagnostic d'espèce et l'estimation du niveau de parasitémie.
a. Identification de l'Étape de l'Anneau :
- P. falciparum : Apparaît comme un point violet avec un anneau fin.
- P. vivax : Tache violette avec un corps déformé.
- P. ovale : Anneau avec un gros point violet.
- P. malariae : Tache violette avec un corps épais.
b. Identification de l'Étape Trophozoïte :
- P. falciparum : Tache plus grande entourant une plus petite.
- P. vivax : Cercle déformé contenant une tache étendue.
- P. ovale : Cercle oval contenant une tache violette.
Recherche d'antigènes spécifiques (immunochromatographie):
- Now® Malaria de Binax: Détecte la protéine HRP-2 sécrétée par les hématozoaires. Haute sensibilité pour P. falciparum (96 %), modérée pour P. vivax (87 %), et insuffisante pour P. malariae et P. ovale (67 %). L'antigénémie HRP-2 peut persister 15 à 30 jours après l'infection.
- OptiMAL-IT®: Teste la présence de pfHRP-2 et pLDH, une enzyme sécrétée par toutes les plasmodies humaines. La pLDH disparaît du sang avec les parasites sous traitement, contrairement à HRP-2. Sensibilité de 92,6 % pour P. falciparum.