Contenu:
◉ Introduction
Toxoplasma gondii est un protozoaire à multiplication intracellulaire obligatoire appartenant au phylum Apicomplexa. Cette anthropozoonose cosmopolite est très fréquente et immunisante. Habituellement bénigne et asymptomatique chez les individus immunocompétents, l'infection par Toxoplasma gondii peut cependant présenter des risques graves dans certaines situations.
Deux contextes présentent des risques particuliers :
- Grossesse : l'infection peut entraîner des fœtopathies graves, menaçant le développement normal du fœtus.
- Immunodépression : les personnes vivant avec le VIH ou les receveurs de greffes d'organes sont à risque de complications sévères.
En raison de ces risques, le dépistage et la prévention de l'infection par Toxoplasma gondii sont systématiques dans ces contextes spécifiques, permettant une gestion adéquate et une réduction des complications associées.
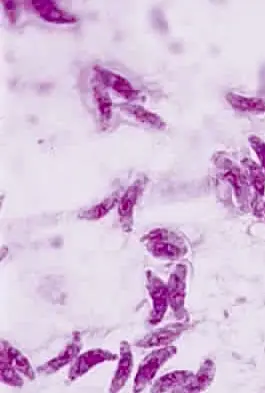
Photo 01: Toxoplasma gondii
◉ Classification
- Règne : Protistes.
- Phylum : Apicomplexa (sporozoaires).
- Classe : Coccidea.
- Ordre : Eimeriorinae.
- Famille : Sarcocystidae.
- Sous-famille : Toxoplasmatinae
- Genre : Toxoplasma.
- Espèce : gondii (1 seule espèce).
◉ Modes de transmission de la toxoplasmose à l'homme
- Ingestion de viande : La majorité des infections humaines survient par ingestion de viande contenant des kystes de Toxoplasma gondii.
- Ingestion de terre, d'eau ou de végétaux contaminés : Les oocystes présents dans l’environnement peuvent contaminer la terre, l'eau ou les végétaux, et leur ingestion peut entraîner une infection.
- Contact direct avec des chats : Plus rarement, l’infection peut se produire par contact direct avec des chats, par exemple via un pelage souillé ou la litière.
- Transmission congénitale : La transmission peut se faire par passage transplacentaire des tachyzoïtes lors d’une phase de parasitémie maternelle, pouvant entraîner des fœtopathies graves.
- Transmission iatrogène : Cela peut se produire par transplantation d’organes solides, et exceptionnellement par transfusion sanguine ou greffe de moelle osseuse.
- Transmission accidentelle : Les accidents de laboratoire peuvent conduire à une inoculation de tachyzoïtes.
◉ Morphologie
Toxoplasma gondii se présente sous trois formes
- Trophozoïte (Tachyzoïte) : forme libre
- Bradyzoïte et kyste : forme quiescente
- Oocyste : résultat du cycle sexué.
◉ 1. Trophozoïte
Le trophozoïte est la forme invasive du parasite, à l’origine des lésions observées au cours de la toxoplasmose. Il a une forme de croissant, avec une extrémité pointue et l'autre arrondie.
- Il mesure de 3 à 9 μm de longueur. Le noyau est ovoïde et est situé à l'extrémité émoussée du parasite.
- Le trophozoïte se colore bien avec la coloration de Giemsa, le cytoplasme apparaissant bleu azur et le noyau rouge.
- Le trophozoïte en multiplication active est observé de manière intracellulaire dans divers tissus pendant la phase aiguë précoce de l'infection. Des trophozoïtes extracellulaires peuvent également être observés.
- Il peut envahir n'importe quelle cellule nucléée et se répliquer à l'intérieur de vacuoles cytoplasmiques par un processus appelé endogonie (bourgeonnement interne), où deux trophozoïtes filles sont formés, chacun entouré d'une membrane, tout en restant à l'intérieur de la cellule parentale. Lorsque la cellule hôte devient distendue par le parasite, elle se désintègre, libérant les trophozoïtes qui infectent d'autres cellules.
- Pendant l'infection aiguë, le trophozoïte en prolifération à l'intérieur de la cellule hôte peut apparaître arrondi et enveloppé par la membrane de la cellule hôte. Cela est appelé pseudo-kyste ou colonie et peut être différencié des kystes tissulaires par des réactions de coloration. Les trophozoïtes en prolifération rapide pendant l'infection aiguë sont appelés tachyzoïtes. Les trophozoïtes sont sensibles au dessèchement, au gel-dégel et à la digestion gastrique.
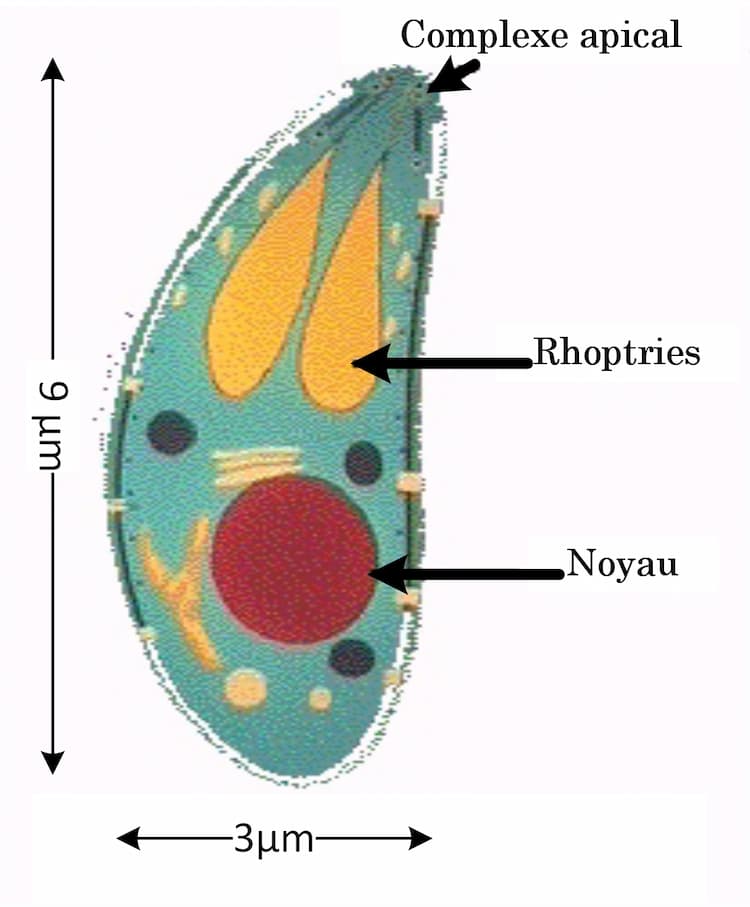
Photo 02: Trophozoïte
◉ 2. Kyste tissulaire
Les kystes tissulaires sont la forme de repos du parasite.
- Ils sont trouvés pendant la phase chronique de l'infection et peuvent être trouvés dans le cerveau (site le plus courant), les muscles squelettiques et divers autres organes.
- La paroi du kyste est éosinophile et se colore avec l'argent, contrairement au pseudo-kyste.
- Avec la coloration au PAS (acide périodique Schiff), la paroi du kyste se colore faiblement, et les parasites à l'intérieur se colorent profondément. Les parasites se multipliant lentement à l'intérieur du kyste sont appelés bradyzoïtes.
- Le kyste est rond ou ovale, de 10 à 20 μm de taille, et contient de nombreux bradyzoïtes. Les kystes restent viables dans les tissus pendant plusieurs années.
- Chez les hôtes immunologiquement normaux, les kystes restent silencieux, mais chez les sujets immunodéprimés, ils peuvent se réactiver, conduisant à une maladie clinique.
- Il est relativement résistant et lorsque la viande crue ou insuffisamment cuite contenant les kystes est consommée, l'infection se produit.
- La paroi du kyste est perturbée par la digestion peptique ou tryptique et les parasites libérés initient l'infection en envahissant les cellules épithéliales intestinales.
- Ils atteignent divers tissus et organes par la dissémination sanguine et lymphatique.
- Les kystes sont sensibles à la dessiccation, au gel et au dégel, et à la chaleur au-dessus de 60 °C.
◉ 3. Oocyste (Reproduction Sexuée)
- La reproduction sexuée de Toxoplasma gondii se déroule dans les cellules épithéliales de l'intestin du chat, qui est l'hôte définitif du parasite.
- Les chatons, après avoir été infectés, excrètent dans leur environnement plus de 10 millions d’oocystes non sporulés par jour pendant une quinzaine de jours. Ces oocystes sont la forme de dissémination du parasite.
- Les oocystes sont ovoïdes, mesurant environ 14 μm de long et 9 μm de large, et possèdent une membrane externe résistante, ce qui les protège dans l'environnement.
- Les oocystes excrétés dans l'environnement doivent sporuler pour devenir infectieux. Ce processus de sporulation dépend de la température, de l'humidité et de la disponibilité en oxygène.
- En conditions favorables, les oocystes deviennent infestants en 1 à 5 jours. Un oocyste sporulé contient deux sporocystes ovoïdes, chacun renfermant quatre sporozoïtes, et peut rester infectieux jusqu'à un an dans l'environnement.
- Cette capacité de résistance et de sporulation permet à Toxoplasma gondii de perdurer et de se propager efficacement dans l'environnement, augmentant ainsi les risques d'infection pour d'autres hôtes.
◉ Cycle Évolutif
T. gondii a deux types de cycles de vie :
◉ 1. Cycle entérique (Cycle félin)
Le cycle entérique se produit chez le chat et les autres hôtes définitifs
- La reproduction sexuée (gamétogonie) et la reproduction asexuée (schizogonie) se produisent toutes deux dans les cellules épithéliales de la muqueuse de l'intestin grêle du chat.
- Le chat acquiert l'infection en ingérant des kystes tissulaires dans la viande de rats et d'autres animaux ou en ingérant des oocystes présents dans ses fèces.
- Les bradyzoïtes sont libérés dans l'intestin grêle et subissent une multiplication asexuée (schizogonie) conduisant à la formation de mérozoïtes.
- Certains mérozoïtes pénètrent dans les tissus extra-intestinaux, entraînant la formation de kystes tissulaires dans d'autres organes du corps.
- D'autres mérozoïtes se transforment en gamétocytes mâles et femelles et le cycle sexuel (gamétogonie) commence, avec la formation de microgamètes et de macrogamètes.
- Un macrogamète est fécondé par un microgamète mobile, entraînant la formation d'un oocyste, qui passe par des étapes de maturation (sporulation) dans le sol après avoir été excrété par l'hôte dans ses fèces.
- Un oocyste mature contenant huit sporozoïtes est la forme infectieuse qui peut être ingérée par des rats ou d'autres mammifères pour répéter le cycle.
◉ 2. Cycle exoentérique (Cycle humain)
Le cycle exoentérique se produit chez les humains, les souris, les rats, les moutons, les bovins, les porcs et les oiseaux, qui sont les hôtes intermédiaires.
- Les sporozoïtes des oocystes et les bradyzoïtes des kystes tissulaires pénètrent dans la muqueuse intestinale et se multiplient asexuellement pour former des tachyzoïtes (endodyogénie).
- Les tachyzoïtes continuent à se multiplier et se propagent localement par le système lymphatique et le sang.
- Certains tachyzoïtes se propagent également à des organes extra-intestinaux distants comme le cerveau, les yeux, le foie, la rate, les poumons et les muscles squelettiques et forment des kystes tissulaires. Les formes à multiplication lente à l'intérieur des kystes tissulaires sont appelées bradyzoïtes, qui restent viables pendant des années.
- Les bradyzoïtes dormants à l'intérieur du kyste peuvent être réactivés en cas d'immunosuppression, causant une nouvelle infection chez l'hôte.
- L'infection humaine est une impasse pour le parasite
- La toxoplasmose humaine est une zoonose.
- Le cycle naturel complet est principalement maintenu par les chats et les souris.
- Les souris mangent des matériaux contaminés par des oocystes présents dans les fèces de chat. Des kystes tissulaires se développent chez les souris.
- Lorsque ces souris sont mangées par les chats, ceux-ci sont infectés et excrètent à nouveau des oocystes dans les fèces.
◉ Caractéristiques Cliniques
Chez les personnes immunocompétentes, l'infection primaire à Toxoplasma gondii est le plus souvent asymptomatique ou présente des symptômes bénins. Toutefois, elle peut être grave chez les femmes enceintes, car le parasite peut traverser la barrière placentaire et infecter le fœtus avant le développement de son immunité. La gravité de la toxoplasmose congénitale est proportionnelle à la précocité de l'infection du fœtus.
Chez les patients immunodéprimés, comme ceux infectés par le VIH ou ayant subi une transplantation, la toxoplasmose peut entraîner des manifestations sévères. Elle représente une infection opportuniste significative, pouvant causer une encéphalite, une choriorétinite, une pneumopathie et une défaillance multisystémique.
◉ Diagnostic biologique
Le diagnostic de la toxoplasmose aiguë est principalement établi par la démonstration de trophozoïtes et de kystes dans les tissus et les liquides corporels et par la sérologie.
◉ 1. Examen direct
Microscopie
Les tachyzoïtes et les kystes tissulaires peuvent être détectés dans divers échantillons, tels que le sang, les expectorations, les aspirations de moelle osseuse, le liquide céphalo-rachidien (LCR), le liquide amniotique et le matériel de biopsie des ganglions lymphatiques, après coloration par Giemsa, PAS ou Gomori methenamine silver (GMS).
Les tachyzoïtes apparaissent comme des structures en forme de croissant avec un cytoplasme bleu et un noyau sombre.
Les tachyzoïtes ou les kystes peuvent également être démontrés efficacement par une technique d'anticorps fluorescents conjugués dans une biopsie tissulaire ou apposition.
Recherche de l'ADN du Parasite par PCR
PCR quantitative en temps réel est devenue la technique de référence pour sa haute sensibilité. Utilise des cibles spécifiques comme le gène B1 et la séquence REP-529 pour une détection efficace.
Isolement du Parasite
- Inoculation à la Souris : Injection de matériel suspect aux souris pour détecter le parasite, complexe et nécessitant des infrastructures spécialisées.
- Culture Cellulaire : Technique délicate, fragile aux contaminations et peu sensible, peu utilisée aujourd'hui.
◉ 2. Sérologie
Détection d'anticorps
Le diagnostic de l'infection aiguë par T. gondii peut être fait en détectant la présence simultanée d'anticorps IgM et IgG.
- Un titre IgG positif (> 1:10) peut être détecté dès 2-3 semaines après l'infection. Le niveau maximal d'anticorps est observé dans le sang 4-8 semaines après l'infection.
- Un titre d'anticorps IgM positif indique une infection primaire précoce. Cepandant, les nouvelles techniques d'immunocapture détectent des IgM 6 mois voire 1 an et plus, après l'épisode infectieux initial.
- Un titre d'IgM négatif et un titre d'IgG positif indiquent une infection ancienne.
- La recherche des IgA et IgE anti-Toxoplasma, dont la cinétique est proche de celle des IgM mais dont la présence est inconstante, n'apparaît pas pertinente pour le diagnostic de la toxoplasmose chez le sujet immunocompétent.
Techniques de Sérologie
- Dye-test (Sabin-Feldman) : Utilise des toxoplasmes vivants et mesure la lyse par les anticorps. Considéré comme le gold standard pour la sensibilité et spécificité, mais complexe et peu utilisé.
- Immunofluorescence Indirecte (IFI) : Utilise des tachyzoïtes fixés pour détecter les anticorps via fluorescence.
- Agglutination Directe et Haute Sensibilité : Détecte les IgG et IgM avec des améliorations pour augmenter sensibilité et spécificité.
- ISAGA : Technique d’immunocapture pour détecter les IgM, IgA, et IgE avec haute sensibilité et spécificité.
- ELISA et Immunoanalyse : Largement utilisées pour détecter et quantifier les IgG, IgM, et IgA via des antigènes extraits de tachyzoïtes.
- Mesure d'Avidité des IgG : Utilisée pour dater l'infection, indiquant une infection récente si l'avidité est faible.
- Immunoblot (Western Blot) : Utilisé pour confirmer la présence d'IgG anti-Toxoplasma et comparer les profils immunologiques entre différents échantillons.
- ELIFA : Utilisée pour des comparaisons de profils immunologiques, similaire à l'immunoblot.
◉ Conclusion
Toxoplasma gondii est un parasite ubiquitaire capable d'infecter une grande variété d'hôtes, y compris les humains. Chez les personnes immunocompétentes, l'infection est généralement asymptomatique ou bénigne. Toutefois, elle peut avoir des conséquences graves chez les femmes enceintes et les personnes immunodéprimées, entraînant des complications telles que la toxoplasmose congénitale ou des infections opportunistes sévères.
Le diagnostic repose sur des tests sérologiques pour détecter les anticorps et des techniques moléculaires comme la PCR pour identifier l'ADN du parasite. La prévention, par des mesures hygiéniques et un suivi médical approprié, est essentielle pour réduire les risques associés à cette infection.