🏾 Contenu :
- Ⅰ. Introduction
- Ⅱ. Composants d'un pH mètres
- Ⅲ. Principe du pH mètres
- Ⅳ. Comment Calibrer / étalonnier un pH mètre?
🏾 Introduction
Un pH-mètre est un appareil, souvent électronique, permettant la mesure du pH (l'acidité ou l'alcalinité) d'une solution à l'aide d'une échelle numérique de 1 à 14. Il est le plus souvent constitué d'un boîtier électronique donnant la possibilité de l'affichage de la valeur numérique du pH et d'une sonde de pH.
En général cette sonde est une électrode combinée, c'est-à-dire qu'elle est constituée de deux électrodes :
- Une dont le potentiel est connu et constant (appelée électrode de référence ).
- Une électrode indicatrice, appelée électrode de verre, dont le potentiel varie avec le pH.
Le potentiel entre ces deux électrodes est nul à pH=7. On peut alors déterminer la valeur du pH par corrélation car la différence de potentiel entre les deux électrodes évolue proportionnellement au pH.
La surveillance des niveaux de pH est une étape importante dans de nombreux domaines : la production de certains aliments, le milieu de culture, les solutions chimiques, le sol, contrôle qualité, etc.

pH-mètre
🏾 Composants d'un pH-mètre
◉ Un pH-mètre est un instrument scientifique qui mesure l'activité des ions hydrogène dans les solutions à base d'eau, indiquant son acidité ou son alcalinité exprimée en pH. Il se compose de deux éléments de base (3 pour certains modèles) :
1- Un appareil de mesure à impédance d'entrée élevée : c’est le corps principal, qui abrite la micropuce utilisée pour traiter les tensions infimes de l'électrode et afficher les mesures effectuées en unités pH sur un écran.
2- La sonde ou l’électrode combinée : composée de 2 électrodes, c'est la partie où la mesure a réellement lieu. La sonde est la partie consommable, sensible et la plus chère du compteur ; et doit être manipulé avec soin. L’électrode combinée se compose d'une électrode de mesure (électrode de verre) et d'une électrode de référence, toutes deux immergées dans la même solution. Afin d'obtenir une valeur de pH définie, l'électrode de référence doit avoir un potentiel stable défini qui est indépendant de la solution mesurée.
- Électrode de référence est constituée d'un élément de référence (par exemple argent/chlorure d'argent) qui est immergé dans un électrolyte défini. Cet électrolyte doit :
- Être en contact avec la solution mesurée à travers, le plus souvent, une jonction céramique poreuse.
- Avoir une concentration élevée en ions qui se traduit par une faible résistance électrique.
- Suffisamment stable sur une large plage de températures.
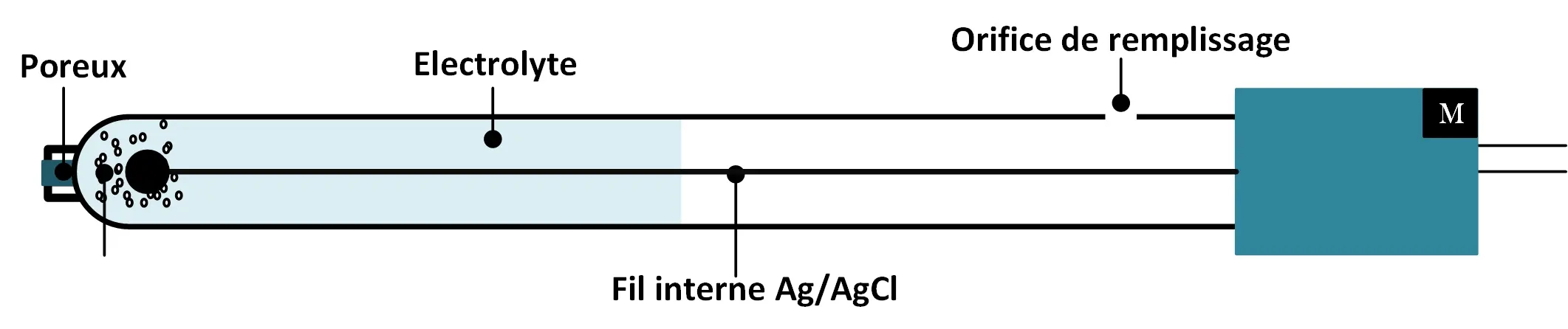
Électrode de reference
- L'électrode de verre du pH : différentes longueurs et formes sont disponibles, de manière à s’adapter aux applications les plus variées. Il est une ampoule en verre sensible aux ions hydrogène, avec une sortie en millivolts qui varie en fonction des variations de la concentration relative des ions hydrogène à l'intérieur et à l'extérieur de l'ampoule.
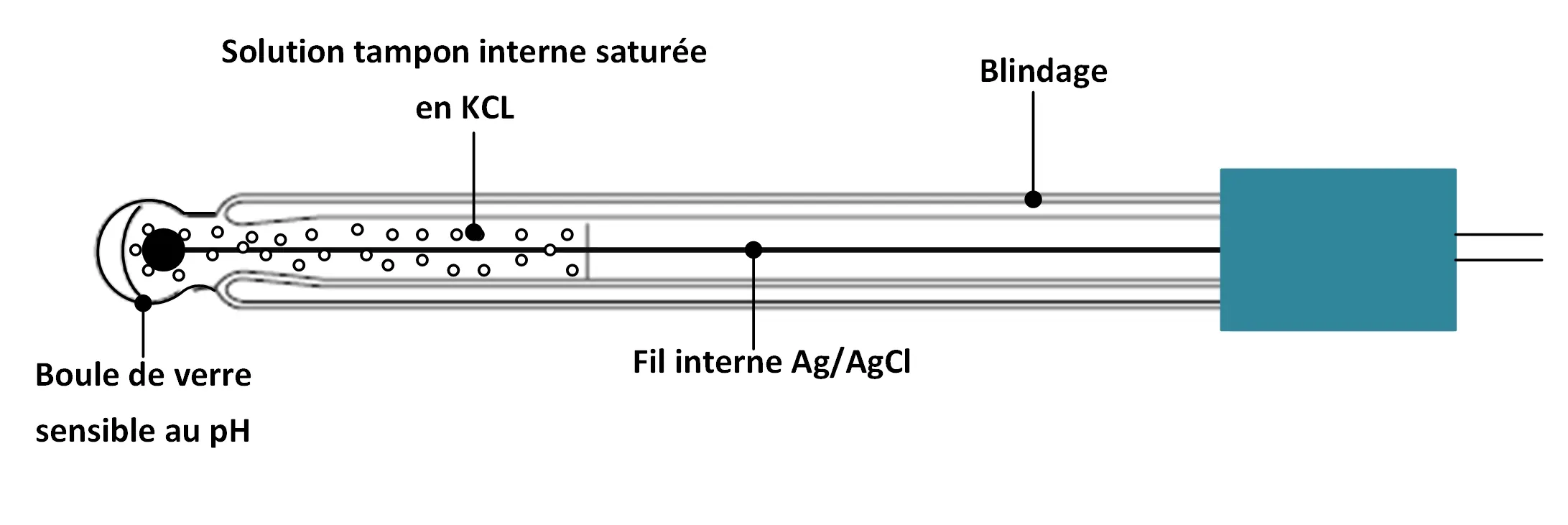
Electrode de verre du pH
3- Sonde de thermomètre : Certains pH-mètres sont équipés de la capacité de mesurer la température de la solution mesurée et d'en tenir compte dans la lecture que le compteur affiche (le pH est directement influencé par la température de la solution). Cette fonction s'appelle ATC, pour "Automatic Temperature Compensation".
🏾 Principe d'un pH-mètre
Le principe de fonctionnement repose sur la mesure du changement de potentiel de tension électronique lorsqu'il est immergé dans la solution testée en mesurant la concentration d'ions hydrogène libres chargés positivement.
L'électrode de verre est remplie d'une solution d'électrolyte qui réagit à la présence d'ions hydrogène. L'électrolyte le fait en acceptant ou en libérant des électrons dans le but de maintenir l'environnement à charge neutre, sans plus de particules chargées positivement que de particules chargées négativement.
Lorsque cela se produit, la quantité d'électrons disponibles dans la solution change. Ce changement est ce que le compteur mesure et extrapole ensuite dans le nombre que vous voyez sur l'affichage du compteur.
🏾 Comment Calibrer / étalonnier un pH mètre?
Laisser tous les tampons atteindre la même température, car les lectures de pH dépendent de la température. Puis, verser environ 30 ml de chacun des tampons pH 10,01, 7,00 et 4,01 dans des béchers séparés de 50 ml. Utilisez ces trois béchers comme béchers de rinçage pendant l'étalonnage.
Rincer d'abord l'électrode de pH avec de l'eau déminéralisée puis dans le bécher de rinçage du tampon pH 10,01.
Placez l'électrode dans le bécher d'étalonnage du tampon pH 10,01, de sorte que la pointe et la jonction de l'électrode soient complètement immergées dans le tampon, et remuez le tampon à une vitesse modérée et uniforme.
Démarrez l'étalonnage sur l'appareil de mesure. Attendre une lecture stable dans le tampon pH 10,01, au moins 1 à 2 minutes.
Une fois la valeur de tampon correcte saisie, passez au point d'étalonnage suivant.
Répétez les étapes avec le tampon 7,00 pH et 4,01