Contenu :
En raison de sa polyvalence, de sa disponibilité et de son coût relativement bas, l'acide acétique est devenu un composé chimique populaire et largement utilisé dans de nombreux aspects de notre vie quotidienne. Cet article fournit plus d'informations sur l'acide acétique, y compris ses propriétés physiques et chimiques, ses diverses méthodes de production et ses applications étendues dans diverses industries.
◉ Définition
L'acide acétique, aussi appelé acide éthanoïque, est un faible acide organique de formule chimique CH3COOH. C'est un liquide incolore qui a une odeur piquante et se trouve couramment dans le vinaigre, qui est généralement une solution diluée d'acide acétique.
Il peut être produit à la fois naturellement (fermentation) et synthétiquement. Il a un rôle de solvant protique, de régulateur d'acidité alimentaire, de conservateur alimentaire antimicrobien et en chimie photographique.
Des solutions plus concentrées peuvent être trouvées en laboratoire. L'acide acétique glacial est une forme hautement concentrée et pure d'acide acétique ne contenant que des traces d'eau (99,4 % d'acide).
Il est important de noter que l'acide acétique peut provoquer des irritations et des brûlures. Par conséquent, il doit être manipulé avec précaution et utilisé à des concentrations et dans des environnements appropriés.
| 64-19-7 | |
| Code produit | LC10100 |
| Formule | C2H4O2 |
| Structure | CH3COOH |
| Synonymes | Acide acétique glacial / alcool de vinaigre / acide carboxylique C2 / acide éthanoïque / acide éthylique / acide méthane carboxylique / acide pyroligneux / acide vinaigré |
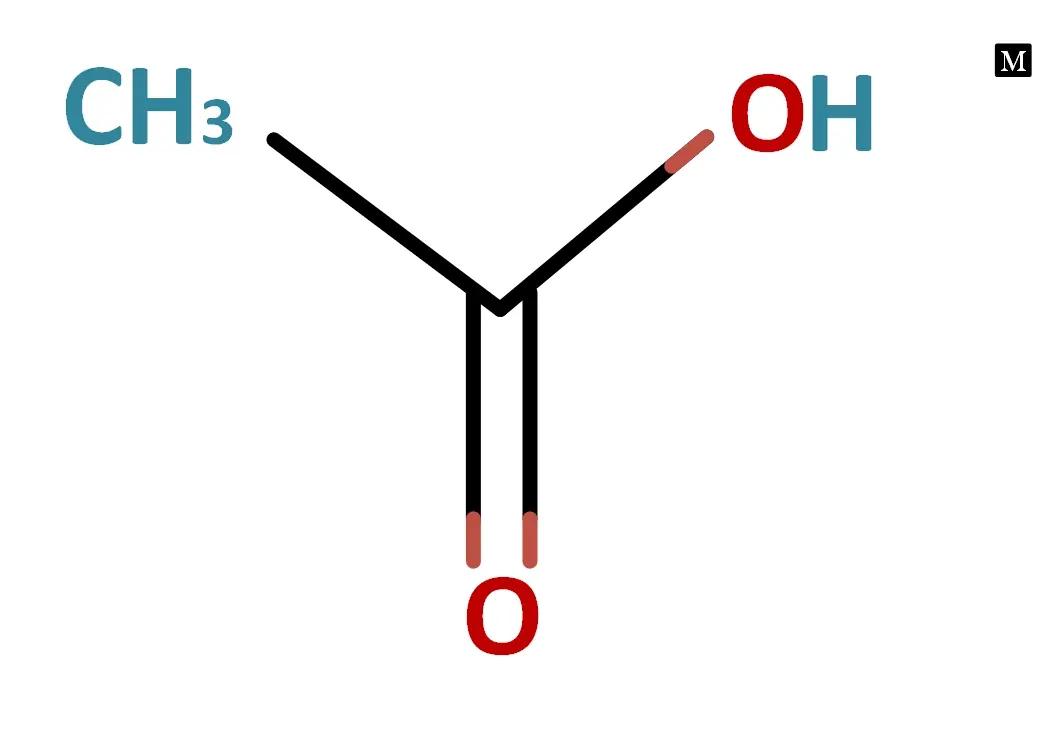
Acide acétique - CH3COOH : représentation de la structure chimique
◉ Propriétés physiques
l'acide acétique est un liquide clair, incolore et combustible avec une odeur âcre de vinaigre. Le seuil d'odeur serait compris entre 0,21 et 1,0 partie par million (ppm). Cette substance est disponible dans le commerce dans des concentrations allant de 6 % à plus de 99 % d'acide, en poids.
Le terme «glacial» dans "acide acétique glacial" fait référence à sa capacité à geler à une température relativement basse, généralement autour de 16,6 degrés Celsius, formant une structure cristalline solide. La température de congélation diminue quand la teneur en eau augmente.
Il est miscible à l'eau et à de nombreux solvants organiques, en particulier l'éthanol, l'oxyde de diéthyle et le glycérol, insoluble dans le sulfure de carbone.
Note : Il est important de noter que ces propriétés peuvent varier en fonction de la concentration de l'acide acétique et des impuretés présentes dans l'échantillon.
◉ L'acidité de l'acide acétique
L'atome d'hydrogène (H) du groupe carboxyle (–COOH) des acides carboxyliques tels que l'acide acétique peut être libéré sous forme d'ion H+ (proton). C'est la capacité à libérer ce proton qui lui confère son acidité. L'acide acétique est un acide faible, mono-protonique en solution aqueuse, avec un pKa d'environ 4,8 à 25 °C.
◉ Production d'acide acétique
La Production d'acide acétique peut être réalisée par deux principales méthodes : la méthode chimique et la méthode fermentaire :
- Méthode chimique (Synthétique) : La voie chimique étant la voie prédominante dans la pratique industrielle actuelle. L'acide acétique peut être produit synthétiquement par diverses méthodes. L'une des méthodes courantes est le procédé de carbonylation du méthanol, dans lequel le méthanol réagit avec le monoxyde de carbone en présence d'un catalyseur.
- Méthode fermentaire : La voie fermentative est principalement adaptée à la génération d'acide acétique de qualité alimentaire. Cette méthode se base sur l'utilisation de microorganismes, généralement des bactéries acétiques du genre Acétobacter ou Gluconacétobacter.
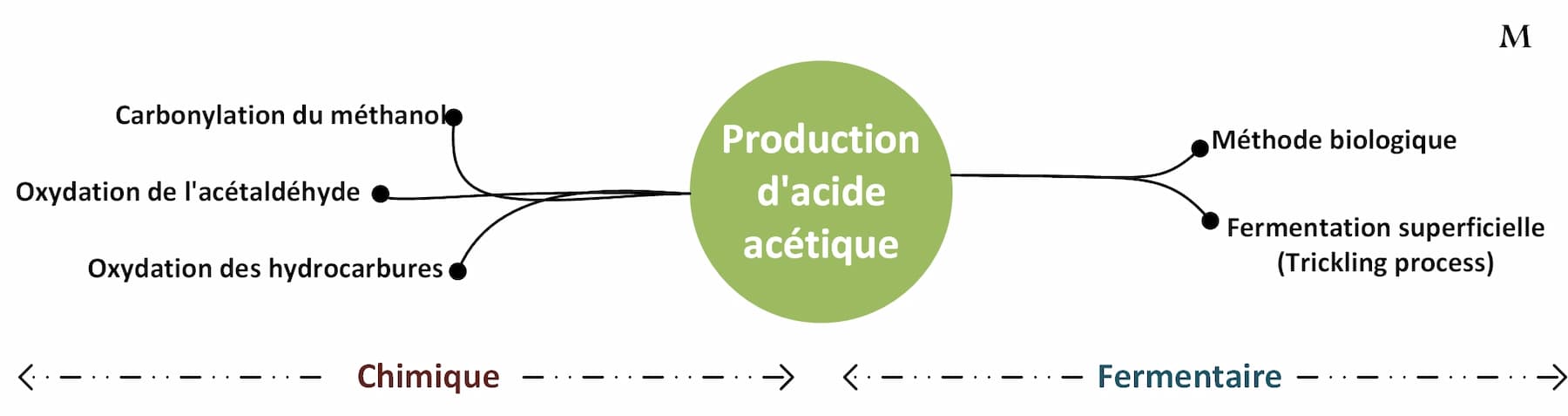
Production d'acide acétique
Il est important de noter que la production d'acide acétique, quelle que soit la méthode utilisée, doit être effectuée dans des installations industrielles appropriées et conformément aux réglementations environnementales et de sécurité.
◉ Utilisation de L'acide acétique
L'acide acétique a de nombreuses utilisations dans différents domaines. Voici quelques-unes des utilisations courantes de l'acide acétique :
- Industrie alimentaire : L'acide acétique est utilisé dans la production alimentaire comme agent de conservation (inhibe la croissance de bactéries), arôme et régulateur de pH. Il est un composant essentiel du vinaigre et est utilisé dans la préparation de divers produits alimentaires tels que les sauces, les marinades et les condiments. Il est considéré comme "de qualité alimentaire" s'il est conforme aux spécifications du Food Chemicals Codex.
- Industrie chimique : L'acide acétique est utilisé comme matière première dans la production d'autres produits chimiques. Il est utilisé dans la fabrication de plastiques, de solvants, d'esters, de colorants et d'autres produits chimiques industriels.
- Textile : L'acide acétique est utilisé dans l'industrie textile pour le processus de teinture et de finition des tissus. Il aide à fixer les colorants sur les fibres et à améliorer la résistance des tissus à la décoloration.
- Nettoyage : En raison de ses propriétés antibactériennes et dégraissantes, l'acide acétique est utilisé dans les produits de nettoyage ménagers. Il est efficace pour éliminer les dépôts de calcaire, les taches et les résidus sur les surfaces.
- Industrie pharmaceutique : L'acide acétique est utilisé dans la production de médicaments, notamment dans la formulation de certains produits pharmaceutiques topiques.
- Laboratoires : Dans les laboratoires, l'acide acétique est utilisé pour ajuster le pH des solutions, préparer des tampons et réaliser des réactions chimiques spécifiques.
- Usage médical : L'acide acétique a plusieurs utilisations médicales : antiseptique, traitement des verrues, examen du col de l'utérus (Visual Inspection with Acetic Acid (VIA)), traitement des otites, etc.
◉ L'acide acétique est-il nocif pour l'homme ?
Lorsqu'il est utilisé correctement et conformément aux directives, l'acide acétique présent dans des produits ménagers courants, tels que le vinaigre de cuisine dilué, est généralement considéré comme sûr et ne devrait pas avoir d'effets néfastes sur la santé.
Cependant, il est important de noter qu'à des concentrations élevées, l'acide acétique est un produit chimique corrosif et peut être nocif pour l'homme s'il est utilisé, manipulé ou ingéré de manière inappropriée. Voici quelques considérations sur sa toxicité :
- Contact cutané : Le contact avec de l'acide acétique concentré peut entraîner des brûlures et une irritation cutanée. Une exposition prolongée ou répétée peut causer des lésions graves à la peau.
- Inhalation : L'inhalation de vapeurs d'acide acétique peut provoquer une irritation des voies respiratoires, des difficultés respiratoires, une toux et une sensation de brûlure dans la gorge. À des concentrations élevées ou en cas d'exposition prolongée, cela peut entraîner des dommages pulmonaires.
- Ingestion : L'ingestion de cet acide concentré peut causer des brûlures sévères dans la bouche, la gorge, l'œsophage et l'estomac. Cela peut entraîner des douleurs abdominales, des vomissements, des difficultés à avaler et des complications potentiellement graves.
- Yeux : Le contact direct de l'acide avec les yeux peut provoquer des brûlures, une irritation sévère, des lésions cornéennes et une diminution de la vision. En cas de contact, un rinçage immédiat et abondant des yeux est essentiel.
Il est essentiel de manipuler l'acide acétique avec précaution et de suivre les mesures de sécurité appropriées, y compris l'utilisation d'équipement de protection individuelle. En cas d'exposition ou de contact, il est important de consulter immédiatement un professionnel de la santé et de suivre les mesures de premiers secours recommandées.